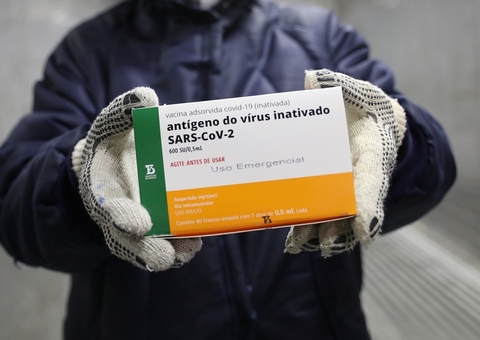
A Agência Nacional de Vigilância Sanitária (Anvisa) deve retirar a obrigatoriedade de ensaios clínicos de fase 3 para conceder registros emergenciais de vacinas contra a Covid-19 no Brasil.
Isso significa que farmacêuticas e laboratórios não precisarão repetir no país testes já feitos e validados em outros locais. As empresas, no entanto, ainda deverão apresentar dados que comprovem a segurança e a eficácia das vacinas.
A medida pode acelerar a aprovação de vacinas como a Sputnik V, produzida pela Rússia e cuja eficácia, segundo resultados preliminares, é de 91,6%. No Brasil, há um acordo com a farmacêutica União Química para fabricar o imunizante.
Com a mudança, a Sputnik V deve receber a autorização para uso emergencial sem a repetição de ensaios na fase 3 no Brasil. Os estudos dessa etapa são feitos com milhares de pessoas, sendo que uma parcela recebe a vacina e outra parte recebe o placebo. Em seguida, os pesquisadores comparam quem se infectou com o novo coronavírus entre o grupo que recebeu a vacina e o grupo que recebeu o placebo.
No caso da Sputnik V, a Anvisa ainda pede que a farmacêutica apresente documentos e dados do estudo que confirmem a eficácia e a segurança da vacina, já aprovada em países da América Latina como Argentina e México.
Brasil
Anvisa deve retirar obrigatoriedade de testes para aprovação de vacinas
Anvisa deve retirar obrigatoriedade de testes para aprovação de vacinas
Artigos relacionados
Últimas notícias
Artigos relacionados
Quer receber todo final de noite um resumo das notícias do dia?
Inscrição confirmada
Obrigado por se inscrever!
Você vai receber no final da noite o resumo das principais notícias do dia.